(波士顿)¬-数以千计的共生微生物生活在人体的粘膜和表皮表面,并且已经确定该微生物组会影响其宿主对多种病原体的耐受性和敏感性。然而,并不是所有生物体都对宿主感染病原体产生了耐受性。例如,已知小鼠的肠道微生物组比人的肠道微生物组更有效地防止某些病原体如鼠伤寒沙门氏菌的感染。

这就提出了一个有趣的可能性,即分析人类与其他物种(例如小鼠)之间的宿主-微生物组相互作用之间的差异,并指出保护或对某些病原体敏感的细菌的个别类型,可能会导致全新的治疗方法。然而,尽管已经在小鼠中很好地研究了肠道微生物组的组成及其对宿主免疫反应的影响,但无法研究微生物组如何在高度限定的条件下直接与肠壁上皮细胞直接相互作用,从而发现特定的细菌菌株可以诱导对传染性病原体的宿主耐受。
现在,由Wyss创始董事Donald Ingber博士领导的协作团队。哈佛大学Wyss生物启发工程研究所的博士和哈佛医学院(HMS)的Dennis Kasper博士利用Wyss的微流控芯片上的器官(Organ Chip)技术来模拟小鼠肠道的不同解剖部分及其共生关系。体外复杂的生活微生物组。研究人员概括了鼠伤寒沙门氏菌对工程小鼠结肠芯片中肠上皮表面的破坏作用,并且在对小鼠和人类微生物群的比较分析中,能够确认共生细菌屎肠球菌有助于宿主耐受鼠伤寒沙门氏菌感染。 。这项研究发表在细胞与感染微生物学前沿。
该项目是在Wyss Institute的DARPA支持的“宿主抗逆性技术”(THoR)项目下启动的,该项目的目的是通过研究某些动物物种和人类之间的差异来发现对感染耐受性的关键作用。Ingber的小组在先前的研究中使用人类结肠芯片显示了源自小鼠和人类粪便的微生物产生的代谢产物如何具有不同的潜力来影响肠道出血性大肠杆菌病原体感染的易感性。
“生物医学研究在很大程度上取决于诸如小鼠之类的动物模型,它们无疑具有巨大的好处,但没有提供机会研究特定器官内的正常和病理过程,例如肠道,特写和实时。丹尼斯·卡斯珀(Dennis Kasper)小组进行的一项重要的概念验证研究强调,我们的工程小鼠肠道芯片平台正是提供了这一功能,并提供了在高度可控的条件下体外研究宿主-微生物组与不同物种的微生物组相互作用的可能性,” Ingber说。“鉴于小鼠免疫学的深层表征,这种能力可以极大地帮助推进目前使用这些动物进行微生物组和宿主反应研究的研究人员的工作。
设计鼠标片上肠道平台
在他们的新研究中,研究小组专注于小鼠肠道。“传统上,很难在任何生物体外模拟宿主-微生物组的相互作用,因为许多细菌严格厌氧并在正常的大气氧气条件下死亡。Organ Chip技术可以重现这些条件,并且更容易获得原代肠道和免疫细胞这项研究的第一作者弗朗西斯卡·加扎尼加加(Francesca Gazzaniga)博士说,他是来自老鼠的,而不是依靠人类活组织检查。
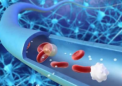
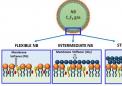
Gazzaniga和她的同事从小鼠肠道不同区域(包括十二指肠,空肠,回肠和结肠)分离出肠隐窝,使它们的细胞通过中间的“有机样”步骤进行培养,其中小组织碎片形成并生长,然后将其接种到Wyss器官芯片的两个平行微流灌注通道之一中,以创建区域特定的肠道芯片。第二个独立灌注的通道模拟血液血管系统,并通过多孔膜与第一个分离,该膜可交换营养成分,代谢产物和肠上皮细胞用来与血管和免疫细胞通讯的分泌分子的交换。
 生物帮
生物帮